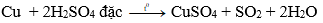Hóa học 9 Bài 17: Dãy hoạt động hóa học của kim loại được THPT Ngô Thì Nhậm biên soạn hy vọng sẽ là là tài liệu hữu ích giúp các em nắm vững kiến thức bài học và đạt kết quả tốt trong các bài thi, bài kiểm tra trên lớp.
Tóm tắt lý thuyết Hóa học 9 Bài 17
I. Dãy hoạt động hóa học của kim loại được xây dựng như thế nào?
Các kim loại được sắp xếp theo chiều giảm dần mức độ hoạt động hóa học :
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au
II. Dãy hoạt động hóa học của kim loại có ý nghĩa như thế nào?
Dãy hoạt động hóa học của kim loại cho biết:
1. Mức độ hoạt động hóa học của các kim loại giảm dần từ trái sang phải.
2. Những kim loại đứng trước Mg là những kim loại mạnh (K, Na, Ba,..), tác dụng với nước ở điều kiện thường tạo thành kiềm và giải phóng H2.
3. Kim loại đứng trước H phản ứng với một số dung dịch axit giải phóng khí H2.
4. Kim loại đứng trước (trừ Na, K…) đẩy kim loại đứng sau ra khỏi dung dịch muối.
Giải bài tập SGK Hóa học 9 Bài 17
Bài 1 (trang 54 SGK Hóa 9)
Dãy kim loại nào sau đây được sắp xếp đúng theo chiều hoạt động hóa học tăng dần?
A. K, Mg, Cu, Al, Zn, Fe.
B. Fe, Cu, K, Mg, Al, Zn.
C. Cu, Fe, Zn, Al, Mg, K.
D. Zn, K, Mg, Cu, Al, Fe.
E. Mg, K, Cu, Al, Fe.
Lời giải:
Chỉ có dãy C gồm các kim loại: Cu, Fe, Zn, Al, Mg, K được sắp xếp theo chiều hoạt động hóa học tăng dần
Bài 2 (trang 54 SGK Hóa 9)
Dung dịch ZnSO4 có lẫn tạp chất là CuSO4. Dùng kim loại nào sau đây để làm sạch dung dịch ZnSO4? Giải thích và viết phương trình phản ứng.
a) Fe.
b) Zn.
c) Cu.
d) Mg.
Lời giải:
b) Zn. Dùng kẽm vì có phản ứng:
Zn + CuSO4 → ZnSO4 + Cu ↓
Nếu dùng dư Zn, Cu tạo thành không tan được tách ra khỏi dung dịch và thu được dung dịch ZnSO4 tinh khiết.
Bài 3 (trang 54 SGK Hóa 9)
Viết các phương trình hóa học:
a) Điều chế CuSO4 từ Cu.
b) Điều chế MgCl2 từ mỗi chất sau: Mg, MgSO4, MgO, MgCO3 (các hóa chất cần thiết coi như có đủ).
Lời giải:
a) Sơ đồ chuyển hóa: Cu → CuO → CuSO4
PTHH: 2Cu + O2 2CuO
CuO + H2SO4 → CuSO4 + H2O
Hoặc: Cu + 2H2SO4đặc CuSO4 + SO2 + 2H2O
b) Cho mỗi chất Mg, MgO, MgCO3 tác dụng với dung dịch HCl, cho MgSO4 tác dụng với BaCl2 ta thu được MgCl2.
Mg + 2HCl → MgCl2 + H2 ↑
MgO + 2HCl → MgCl2 + H2O
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
MgSO4 + BaCl2 → MgCl2 + BaSO4 ↓.
Bài 4 (trang 54 SGK Hóa 9)
Hãy cho biết hiện tượng nào xảy ra khi cho:
a) Kẽm vào dung dịch đồng clorua.
b) Đồng vào dung dịch bạc nitrat.
c) Kẽm vào dung dịch magie clorua.
d) Nhôm vào dung dịch đồng clorua.
Viết các phương trình phản ứng hóa học nếu có.
Lời giải:
Hiện tượng xảy ra:
a) Zn tan dần, dung dịch CuCl2 nhạt màu xanh, chất rắn màu đỏ bám vào viên kẽm.
CuCl2 + Zn → ZnCl2 + Cu ↓
b) Cu tan dần, chất rắn màu trắng bám vào bề mặt đồng (Đồng đẩy được Ag ra khỏi dung dịch muối), màu xanh lam dần xuất hiện trong dung dịch.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
c) Không có hiện tượng gì xảy ra và không có phản ứng.
d) Al tan dần, màu xanh lam của dung dịch nhạt dần, có chất rắn màu đỏ bám vào bề mặt nhôm.
2Al + 3CuCl2 → 2AlCl3 + 3Cu ↓
Bài 5 (trang 54 SGK Hóa 9)
Cho 10,5g hỗn hợp hai kim loại Cu, Zn vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc).
a) Viết phương trình hóa học.
b) Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng.
Lời giải:
a) Phương trình hóa học của phản ứng:
Zn + H2SO4 loãng → ZnSO4 + H2
Cu đứng sau H trong dãy hoạt động hóa học nên không phản ứng với dung dịch H2SO4 loãng
b) Chất rắn còn lại là Cu
Theo pt nZn = nH2 = 0,1 mol ⇒ mZn = 65.0,1 = 6,5g
Khối lượng chất rắn còn lại: mCu = 10,5 – 6,5 = 4g.
Trắc nghiệm Hóa học 9 Bài 17 (có đáp án)
Câu 1: Dãy kim loại được sắp xếp theo chiều hoạt động hóa học giảm dần:
A. Na, Mg, Zn
B. Al, Zn, Na
C. Mg, Al, Na
D. Pb, Al, Mg
Đáp án: A
Câu 2: Từ Cu và hoá chất nào dưới đây để thu được CuSO4 ?
A. MgSO4
B. Al2(SO4)3
C. H2SO4 loãng
D. H2SO4 đặc, nóng
Đáp án: D
Câu 3: Có một mẫu dung dịch MgSO4 bị lẫn tạp chất là ZnSO4, có thể làm sạch mẫu dung dịch này bằng kim loại
A. Zn
B. Mg
C. Fe
D. Cu
Đáp án: B
Sử dụng một lượng dư kim loại Mg
Mg + ZnSO4 → MgSO4 + Zn ↓
Lọc bỏ kim loại thu được dung dịch MgSO4 tinh khiết.
Câu 4: Dãy kim loại tác dụng được với dung dịch Cu(NO3)2 tạo thành Cu kim loại:
A. Al , Zn, Fe
B. Zn, Pb, Au
C. Mg, Fe , Ag
D. Na, Mg , Al
Đáp án: A
Các kim loại tác dụng được với Cu(NO3)2 tạo thành Cu kim loại phải đứng trước Cu trong dãy hoạt động hóa học của kim loại và các kim loại đó phải không tác dụng với nước.
→ A thỏa mãn.
Câu 5: Có một mẫu Fe bị lẫn tạp chất là nhôm, để làm sạch mẫu sắt này bằng cách ngâm nó với
A. Dung dịch NaOH dư
B. Dung dịch H2SO4 loãng
C. Dung dịch HCl dư
D. Dung dịch HNO3 loãng .
Đáp án: A
Sử dụng một lượng dư dung dịch NaOH
2Al + 2H2O + 2NaOH → 2NaAlO2 + 3H2
Lọc lấy kim loại rửa sạch thu được Fe tinh khiết.
Chú ý: Một số kim loại như Al, Zn … có thể tác dụng được với dung dịch kiềm.
Câu 6: Cho 4,8 gam kim loại M có hóa trị II vào dung dịch HCl dư , thấy thoát ra 4,48 lít khí hiđro (ở đktc). Vậy kim loại M là :
A. Ca
B. Mg
C. Fe
D. Ba
Đáp án: B
nkhí = 4,48 : 22,4 = 0,2 mol
Vậy kim loại cần tìm là Mg.
Câu 7: Hiện tượng gì xảy ra khi cho 1 thanh đồng vào dung dịch H2SO4 loãng?
A. Thanh đồng tan dần, khí không màu thoát ra
B. Thanh đồng tan dần, dung dịch chuyển thành màu xanh lam
C. Không hiện tượng
D. Có kết tủa trắng.
Đáp án: C
Đồng đứng sau H trong dãy hoạt động hóa học của kim loại nên không tác dụng với H2SO4 loãng.
Câu 8: Hiện tượng xảy ra khi cho 1 lá nhôm vào dung dịch H2SO4 đặc, nguội:
A. Khí mùi hắc thoát ra
B. Khí không màu và không mùi thoát ra
C. Lá nhôm tan dần
D. Không có hiện tượng
Đáp án: D
Chú ý: Một số kim loại như Al, Fe, Cr … không tác dụng với H2SO4 đặc, nguội.
Câu 9: Cho 5,4 gam nhôm vào dung dịch HCl dư , thể tích khí thoát ra (ở đktc) là:
A. 4,48 lít
B. 6,72 lít
C. 13,44 lít
D. 8,96 lít
Đáp án: B
Số mol Al = 5,4 : 27 = 0,2 mol
→ Vkhí = 0,3.22,4 = 6,72 lít.
Câu 10: Cho 1 viên Natri vào dung dịch CuSO4, hiện tượng xảy ra:
A. Viên Natri tan dần, sủi bọt khí, dung dịch không đổi màu
B. Viên Natri tan dần,không có khí thoát ra, có kết tủa màu xanh
C. Viên Natri tan, có khí không màu thoát ra, xuất hiện kết tủa màu xanh
D. Không có hiện tượng.
Đáp án: C.
Viên Natri tan, có khí không màu thoát ra, xuất hiện kết tủa màu xanh lam
PTHH:
2Na + 2H2O → 2NaOH + H2 ↑
2NaOH + CuSO4 → Cu(OH)2 (↓ xanh) + Na2SO4.
******************
Trên đây là nội dung bài học Hóa học 9 Bài 17: Dãy hoạt động hóa học của kim loại do THPT Ngô Thì Nhậm biên soạn bao gồm phần lý thuyết, giải bài tập và các câu hỏi trắc nghiệm có đáp án đầy đủ. Hy vọng các em sẽ nắm vững kiến thức về Dãy hoạt động hóa học của kim loại. Chúc các em học tập thật tốt và luôn đạt điểm cao trong các bài thi bài kiểm tra trên lớp.
Biên soạn bởi: Trường THPT Ngô Thì Nhậm
Chuyên mục: Hoá học 9